Злокачественные новообразования
В подавляющем большинстве случаев злокачественные опухоли развиваются у генетически предрасположенных лиц, на которых в какой-то промежуток времени воздействовали средовые канцерогенные факторы. Возникновение таких форм рака не подвержено наследованию по закону Менделя (мультифакториальные или спорадические формы).
Некоторые формы рака обусловлены мутациями в одном гене (моногенные) и наследуются по законам Менделя (наследственные или семейные формы). Наследственную природу имеют ретинобластома, нейробластома, опухоль Вильмса, семейный полипоз толстой кишки, некоторые формы рака молочной железы и многие другие.
■ Ретинобластома — довольно распространённая злокачественная опухоль у детей, наследуемая по аутосомно-доминантному типу (180200, ген RB1, 13q14.1-q14.2) с пенетратностью более 90% (то есть только у 10% носителей мутантного гена роста опухоли нет). Эта опухоль развивается в раннем детском возрасте из нервных клеток сетчатки глаза. Обнаружить диагностическую мутацию довольно сложно. Приблизительно 85% составляют одиночные точечные мутации, которые можно идентифицировать только прямыми молекулярно-генетическими методами. В случае ранней диагностики ретинобластомы и своевременного лечения вероятность выживания и сохранения зрения поражённого глаза (глаз) довольно высока.
■ Семейный полипоз толстой кишки (*114500, 5q21, ген APC, ЭД) характеризуется множественными аденоматозными полипами толстой кишки. Полипы появляются в раннем возрасте и чаще локализуются в ректо-сигмовидной области. Ген семейного полипоза АРС в настоящее время клонирован. Наследуемые мутации гена АРС приводят к возникновению рака в 100% случаев [Rozen P. et al., 1999]. При семейном полипозе толстой кишки также могут наблюдаться папиллярная карцинома щитовидной железы, опухоли мозга, саркомы, опухоли тонкой кишки, желудка, гепатобластомы, карцинома поджелудочной железы. Близкие родственники больных семейным полипозом толстой кишки должны обследоваться на предмет выявления мутаций в гене и находиться под постоянным врачебным контролем с 10-12-летнего возраста.
■ Семейная форма рака молочной железы составляет приблизительно 5% всех случаев заболевания. Основные гены предрасположенности к развитию рака молочной железы — BRCA1 (113705, 17q21, ЭД) и BRCA2. Анализ участков хромосом, содержащих гены BRCA1 и BRCA2, в образцах опухолей больных с наследственно обусловленным раком молочной железы выявил потери нормального (не мутированного) алле-ля, что позволило классифицировать BRCA1 и BRCA2, как гены-суп-рессоры опухоли [Bell D.W. et al., 2002]. В клетках, лишённых генов BRCA1 или BRCA2, накапливаются хромосомные аномалии, нарушается контроль за целостностью генома и транскрипцией генов, они становятся более чувствительными к радиационному облучению, что в конечном итоге способствует хромосомной нестабильности и злокачественной трансформации клетки [Davies A.A. et al., 2001]. Выделение генов, ответственных за наследственную предрасположенность к раку
молочной железы, создало принципиально новые возможности медико-генетического консультирования и профилактики заболевания. При обнаружении мутантных генов BRCA1 и/или BRСA2 методом ДНК-диагностики риск рака молочной железы составляет 80-90% [Ford D. et al., 1998]. Проведение периодических осмотров носителей мутаций позволяет своевременно выявить начало заболевания, что обеспечивает эффективное лечение. В ряде исследований показана высокая эффективность профилактической мастэктомии у женщин с наличием перечисленных мутаций. Поэтому своевременное выявлени мутаций и хирургическое вмешательство рассматриваются в настоящее время как высокоэффективные методы профилактики рака молочной железы [Grann V.R. et al., 1998; Hartmann L.C. et al., 1999; Rebbeck T.R. et al., 1999]. Кроме того, доказана профилактическая эффективность приёма тамоксифена в отношении риска развития злокачественных новообразований молочной железы у женщин с генетически повышенным риском этого заболевания [Fisher B. et al., 1998]. Другие гены, обуславливающие предрасположенность к раку молочной железы, представлены в табл..
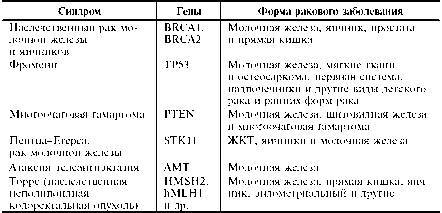
Таблица Наследственные синдромы, ассоциированные с повышенным риском развития рака молочной железы
Таблица Наследственные синдромы, ассоциированные с повышенным риском развития рака молочной железы
■ Наследственные факторы имеют важное значение в развитии рака предстательной железы. Приблизительно у 10% пациентов выявляют мутации в генах высокого риска развития рака предстательной железы; у 20-40% — в генах, обусловливающих умеренный риск заболевания [Schaid D.J. et al., 1998]. Недавно клонирован ген НРС2, ряд мутаций которого приводит к высокому риску рака предстательной железы (приблизительно 10-кратное увеличение по отношению к среднепо-пуляционному); другая часть мутаций увеличивает риск заболевания только в 2-3 раза [Tavtigian S.V. et al., 2001]. Приблизительно 5% случаев семейной формы рака предстательной железы связаны с мутациями гена BRCA2, обусловливающего наследственную предрасположенность
к раку молочной железы. Умеренный риск рака предстательной железы ассоциирован с числом триплетных GAG повторов в гене рецептора андрогенов AR, вариантами генов SRD5A2, GST и полиморфизмом в районе ARE1 простатспецифического Аг [Gsur A. et al., 2002; Nam R.K. et al., 2001]. Получены многообещающие результаты по исследованию связи рака предстательной железы с геном MSR1 (SR-A), который находится на хромосоме 8 (8р22).
■ МЭН. Известно несколько типов МЭН, все они наследуются по ауто-сомно-доминантному типу. Тип I (синдром Вермера, *131100, 11q13, ген MEN1, ЭД) характеризуется развитием опухолей паращитовидных желёз, островков Лангерганса поджелудочной железы и гипофиза. Тип IIa (синдром Сиппла, #171400, 10q11.2, онкоген ret, [164761], ЭД) и IIb (#162300, 10q11.2, онкоген RET, ЭД) чаще всего проявляется медуллярной карциномой щитовидной железы, а также феохромоцитомой и гиперплазией парщитовидных желёз. В развитых странах широкое распространение получил генетический скрининг на выявление предрасположенности к развитию медуллярного рака щитовидной железы, который наиболее часто развивается в рамках МЭН IIa (выявление мутаций RET-мутации). Материалом для анализа служат лейкоциты крови пациента и биопсийный материал щитовидной железы. В случае выявления мутации в лейкоцитах периферической крови можно быть уверенным в том, что у данного пациента медуллярный рак щитовидной железы является проявлением МЭН IIa или имеет семейный-характер. При отсутствии мутации RET-протоонкогена в лейкоцитах и наличии её в самой опухоли с большой уверенность можно говорить о спорадическом медуллярном раке щитовидной железы. Если мутация отсутствует как в лейкоцитах, так и в самой опухоли, окончательного заключения сделать невозможно и необходимо наблюдать пациента.
В табл. приведены другие частые наследственные формы злокачественных новообразований и соответствующие им генетические нарушения. Следует отметить, что установление типа мутации при острых лейкозах, может быть использовано для определения прогноза течения заболевания. Так, при наличии транслокации (8, 21) у больных с лейкозом М2 по ФАБ-классификации, инверсии в 16 хромосоме при М4 лейкозе, транслокации (8, 21) при М3 лейкозе прогноз хороший; в то время как при инверсии в 3 хромосоме у больных с М1 или М4 лейкозами, генетических мутациях в 11q23 при М4 и М5 лейкозах — плохой.
Таблица Хромосомные нарушения при различных новообразованиях
Таблица Хромосомные нарушения при различных новообразованиях

Окончание табл.
Окончание табл.
