Липопротеин (a) в сыворотке крови
Референтные величины содержания липопротеина (а) [ЛП(а)] в сыворотке крови — 0-30 мг/дл.
ЛП(а) состоит из апо(а), который является по своей природе гликопро-теином и ковалентно связан с апо-В100. ЛП(а) имеет значительное структурное сходство с плазминогеном. ЛП(а) крупнее ЛПНП, но обладает по сравнению с ними большей плотностью и имеет электрофоретическую подвижность пре-Р-ЛП. По липидному составу ЛП(а) не отличается от ЛПНП, но белка в ЛП(а) больше. ЛП(а) синтезируется в печени. Все современные иммунохимические методы определения ЛП(а) на самом деле выявляют белок — апо(а).
Повышенная концентрация ЛП(а) в сыворотке крови — фактор риска развития ИБС. По данным литературы, усреднённое содержание апо(а) в крови пациентов с ИБС составляет 12 мг/дл. У 2/3 пациентов развитие атеросклероза зависит от присутствия в крови повышенных концентраций ЛП(а). Установлена тесная корреляция между концентрацией ЛП(а) в сыворотке крови и развитием ИБС. Эпидемиологические исследования показали, что у лиц с нормальной концентрацией ХС, но повышенным содержанием ЛП(а) (выше 30 мг/дл) риск развития ИБС по меньшей степени в 2 раза выше. Риск возрастает в 8 раз, если одновременно повышены концентрации ЛПНП и ЛП(а). ИМ развивается в 4 раза чаще у лиц молодого возраста, к которых содержание апо(а) превышает 48 мг/дл. У пациентов с облитерирующим атеросклерозом содержание апо(а) также повышено.
Концентрация ЛП(а) в крови возрастает после хирургических операций, у больных с онкологическими заболеваниями, при сахарном диабете, острой фазе ревматизма.
Сходство строения апо(а) и белков острой фазы позволяет рассматривать его как специфический белок острой фазы при деструктивных атеро-склеротических процессах в сосудистой стенке. Определение ЛП(а) — тест оценки активности атеросклеротического процесса. Его содержание в крови коррелирует с площадью атероматозного поражения аорты, уровнем гипергликемии, временем свёртывания крови и маркёрами недостаточности экскреторной функции почек. Артериальная гипертензия при атеросклерозе часто сочетается с повышением в крови концентрации ЛП(а).
Концентрация ЛП(а) в крови генетически детерминирована, и в настоящее время не существует ЛС, снижающих её. В связи с этим единственная стратегия лечения пациентов с повышенной концентрацией ЛП(а) — устранение всех прочих факторов риска ИБС (курение, избыточная масса тела, артериальная гипертензия, высокая концентрация ЛПНП).
Эффективность приведённых выше методов исследования для диагностики нарушений липидного статуса представлена в табл..
В настоящее время установлена чёткая корреляция между концентрацией общего ХС в крови и смертностью от сердечно-сосудистых заболеваний. При содержании ХС в крови ниже 200 мг/дл (5,2 ммоль/л) риск развития атеросклероза наименьший. Если концентрация ЛПНП-ХС в крови ниже 100 мг/дл (2,59 ммоль/л), поражения сердца возникают очень редко. Повышение ЛПНП-ХС выше 100 мг/дл отмечают при употреблении пищи, богатой животными жирами и ХС. Неправильное питание, курение и артери
альная гипертензия — синергически действующие факторы, повышающие риск ИБС. Сочетание одного из этих факторов с любым другим примерно на 10 лет ускоряет развитие коронарного атеросклероза критической степени. Снижение концентрации общего ХС в крови и повышение ЛПВП-ХС уменьшает темпы прогрессирования атеросклероза. Снижение концентрации общего ХС в крови на 10% приводит к уменьшению смертности от заболеваний сердца на 20% [Levine G.N. et al., 1995]. Повышение концентрации ЛПВП-ХС на 1 мг/дл (0,03 ммоль/л) снижает риск коронарной патологии на 2-3% у мужчин и женщин. Кроме того, вне зависимости от содержания общего ХС в крови (в том числе и превышающего 5,2 ммоль/л) сохраняется обратная зависимость между содержанием ЛПВП-ХС и частотой сердечной патологии. Концентрации ЛПВП-ХС (менее 1,3 ммоль/л) и ТГ в крови — независимые прогностические показатели вероятности смерти от ИБС [Байни Р., Сперов Л., 2001]. Поэтому содержание ЛПВП-ХС следует считать более точным прогностическим показателем в отношении смертности от ИБС, чем концентрацию общего ХС.
Таблица Эффективность лабораторных тестов для диагностики нарушений ли-пидного статуса
Таблица Эффективность лабораторных тестов для диагностики нарушений ли-пидного статуса
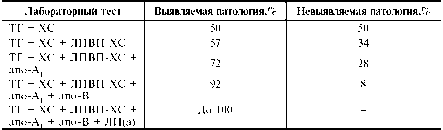
В клинической практике следует учитывать следующие аспекты.
■ Снижение концентрации ЛПНП-ХС и повышение концентрации ЛПВП-ХС способствует уменьшению частоты атеросклероза.
■ Соотношение «общий ХС/ЛПВП-ХС» в норме составляет 3,4, к 75-89 годам оно повышается до 4,7; оптимальным считают соотношение 3,5, а при величинах 5 и более риск ИБС значительно возрастает.
■ Липидный профиль непосредственно связан с доминированием тестостерона у мужчин и эстрогенов у женщин.
■ Концентрация ЛП(а) в сыворотке крови отражает активность атеро-склеротического процесса.
■ Избыточное питание, ожирение, курение и низкая физическая активность оказывают неблагоприятное воздействие на липидный профиль.
■ Коррекция липидных нарушений должна предусматривать не просто снижение концентрации ХС, но и нормализацию неблагоприятного липидного профиля.
■ Снижение массы тела и физические упражнения концентрацию ЛПВП в крови повышают, а ЛПНП-ХС и ТГ — снижают.
■ Развитие атеросклероза начинается ещё в молодом возрасте, поэтому его проявления на более поздних этапах жизни можно предотвратить, ведя здоровый образ жизни с юных лет.
Оптимальный холестерин-липопротеиновый профиль предусматривает следующий уровень показателей в сыворотке крови.
■ Общий ХС — менее 200 мг/дл (5,2 ммоль/л).
■ ЛПВП-ХС — более 50 мг/дл (1,3 ммоль/л).
■ ЛПНП-ХС — менее 130 мг/дл (3,4 ммоль/л).
■ ТГ — менее 250 мг/дл (2,3 ммоль/л).