Антидиуретический гормон в плазме крови
АДГ — пептид, состоящий из 9 аминокислотных остатков. Он синтезируется как прогормон в гипоталамических нейронах, тела которых располагаются в супраоптических и паравентрикулярных ядрах. Ген для АДГ кодирует также нейрофизин II, белок-переносчик, транспортирующий АДГ по аксонам нейронов, которые оканчиваются в задней доле гипофиза, где происходит накопление АДГ. АДГ имеет суточный ритм секреции (её повышение наблюдают ночью). Секреция гормона уменьшается в положении лёжа, при переходе в вертикальное положение его концентрация повышается. Зависимость уровня АДГ в крови от осмолярности показана в табл.. Все перечисленные факторы необходимо учитывать при оценке результатов исследований.
Таблица Референтные величины концентрации АДГ в плазме крови [Тиц У., 1997]
Таблица Референтные величины концентрации АДГ в плазме крови [Тиц У., 1997]

Выход АДГ из накопительных везикул регулируется в первую очередь ос-молярностью плазмы. Средний уровень осмолярности плазмы в норме составляет 282 мосм/л с отклонениями в ту или иную сторону до 1,8%. Если осмолярность плазмы поднимается выше критического уровня (порога) 287 мосм/л, то выход АДГ резко ускоряется, что связано с активацией осморецепторов, расположенных на клеточной мембране супраоптическо-го и паравентрикулярных нейронов гипоталамуса и клетках каротидного синуса на сонных артериях. Данные рецепторы способны уловить изменения осмолярности в плазме крови порядка 3-5% выше средней величины, особенно при резких изменениях (более 2% в час). Быстрое увеличение осмолярности плазмы лишь на 2% приводит к усилению секреции АДГ в 4 раза, тогда как уменьшение осмолярности на 2% сопровождается полным прекращением секреции АДГ.
Гемодинамические факторы также оказывают выраженное регуляторное влияние на секрецию АДГ. Снижение среднего артериального давления и/или «эффективного» объёма плазмы менее чем на 10% могут быть обнаружены барорецепторами, расположенными в клетках левого предсердия и, в меньшей степени, в каротидном синусе. По мультисинаптическому афферентному пути импульсы от «растянутых» барорецепторов передают информацию нейронам супраоптического и паравентрикулярного ядер гипоталамуса, которые стимулируют выход АДГ.
Главный биологический эффект АДГ заключается в увеличении резорбции свободной воды из мочи, находящейся в просвете дистальной части почечных канальцев, в клетки канальцев. АДГ связывается со специфическими V2-рецепторами на наружной мембране этих клеток, вызывая активацию аденилатциклазы, которая образует цАМФ. цАМФ активирует
протеинкиназу А. Протеинкиназа А фосфорилирует белки, которые стимулируют экспрессию гена аквапорина-2, одного из белков, создающих каналы для воды. Аквапорин-2 мигрирует к внутренней поверхности мембраны тубулярных клеток, где встраивается в мембрану, формируя поры или каналы, через которые вода из просвета дистальных канальцев свободно диффундирует внутрь тубулярной клетки. Затем вода проходит из клетки через каналы в плазматической мембране в интерстициальное пространство, откуда поступает в сосудистое русло .
Несахарный диабет (недостаточность АДГ). Истинный несахарный диабет характеризуется полиурией и полидипсией в результате недостаточности АДГ. К стойкому несахарному диабету приводят деструкция надзри-тельного и околожелудочковых ядер или перерезка надзрительного пути выше срединного возвышения.
Причиной заболевания может служить поражение нейрогипофиза любого генеза. Чаще всего это опухоли — краниофарингомы и глиомы зрительного нерва. У больных гистиоцитозом несахарный диабет развивается в 25-50% случаев. Изредка причиной несахарного диабета служат энцефалит, саркоидоз, туберкулёз, актиномикоз, бруцеллёз, малярия, сифилис, грипп, ангина, все виды тифов, септические состояния, ревматизм, лейкоз. Несахарный диабет может развиться после черепно-мозговой травмы, особенно если она сопровождается переломом основания черепа.
Несахарный диабет, развивающийся после хирургических вмешательств на гипофизе или гипоталамусе, может быть как транзиторным, так и постоянным. Течение заболевания, возникающего после случайной травмы, непредсказуемо; спонтанные выздоровления могут отмечаться через несколько лет после травмы.
В последние годы показано, что несахарный диабет может иметь аутоиммунное происхождение (наличие АТ к АДГ-секретирующим клеткам). В редких случаях он может быть наследственным. Несахарный диабет может быть компонентом редко встречающегося синдрома Вольфрама, при котором он сочетается с сахарным диабетом, атрофией зрительных нервов и нейросенсорной тугоухостью.
Клинические признаки полиурии появляются, когда секреторная способность гипоталамических нейронов снижается на 85% [Дедов И.И., 1995]. Недостаточность АДГ бывает полной или частичной, что определяет степень полидипсии и полиурии.
Исследование концентрации АДГ в плазме крови не всегда необходимо для диагностики несахарного диабета. Целый ряд лабораторных показателей довольно точно указывают на наличие у пациента недостаточности секреции АДГ. Суточный объём мочи достигает 4-10 л и более, её плотность колеблется в пределах 1,001-1,005, осмолярность — в пределах 50-200 мосм/л. В периоды выраженной дегидратации плотность мочи повышается до 1,010, а осмолярность до 300 мосм/л. У детей начальным признаком заболевания может быть никтурия. В остальных отношениях функция почек не нарушена. Часто выявляют гиперосмолярность плазмы (выше 300 мосм/л), гипернатриемию (более 155 ммоль/л) и гипокалиемию. При проведении теста с ограничением воды у больных с выраженной недостаточностью АДГ отмечается повышение осмолярности плазмы крови, но осмолярность мочи обычно остаётся ниже осмолярности плазмы крови.
Рис. Секреция и эффекты АДГ
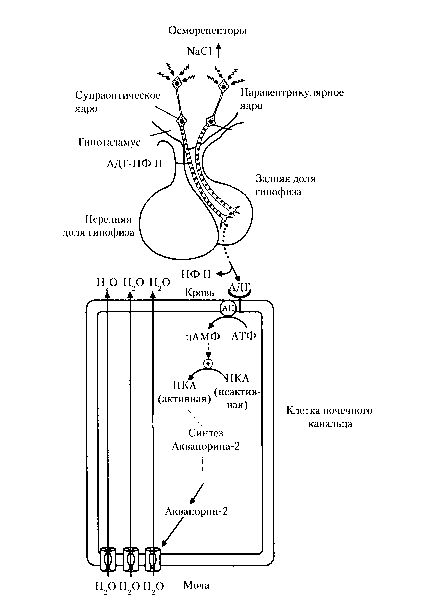
Рис. Секреция и эффекты АДГ
При введении вазопрессина осмолярность мочи быстро повышается. При умеренно выраженной недостаточности АДГ и полиурии осмолярность мочи в ходе теста может быть несколько выше осмолярности плазмы, а реакция на вазопрессин ослаблена.
Постоянно низкие концентрации АДГ в плазме крови (менее 0,5 пг/л) свидетельствуют о выраженном нейрогенном несахарном диабете, субнормальные уровни (0,5-1 пг/л) в сочетании с гиперосмолярностью плазмы — о частичном нейрогенном несахарном диабете. Определение концентрации АДГ в плазме крови — главный критерий, позволяющий дифференцировать частичный несахарный диабет от первичной полидипсии.
Первичный ночной энурез (недостаточность АДГ). Ночной энурез выявляют у каждого десятого ребёнка в возрасте 5-7 лет, а в возрасте 10 лет — у каждого двадцатого. Причиной энуреза могут стать многие факторы: стресс, урогенитальные инфекции, нефрологические нарушения и др. Довольно часто ночное недержание мочи оказывается лишь следствием другого заболевания, но в ряде случаев оно обусловлено первичным ночным энурезом. Этот диагноз ставят у детей старше 5 лет, которые, при отсутствии органических нарушений и нормальном мочеотделении в течение дня, мочатся в постель ночью чаще 3 раз в неделю. Физиологическая особенность организма таких пациентов — низкая концентрация в крови АДГ. Существует наследственная предрасположенность к развитию первичного ночного энуреза. Девочки болеют несколько реже, чем мальчики.
У больных с первичным ночным энурезом в ночное время образуется в 2-3 раза больше мочи, чем у здоровых детей. Важнейшую роль в этом процессе играет АДГ. Его уровень в организме постоянно колеблется. У здорового ребёнка ночью концентрация АДГ в крови выше, чем днём, а при первичном ночном энурезе этот уровень, и без того достаточно низкий, ночью снижается ещё больше, в результате чего образуется большое количество неконцентрированной мочи. Обычно уже к четырем часам утра, гораздо раньше, чем у здоровых детей, мочевой пузырь у больных оказывается заполненным до предела. Сон в это время очень глубокий, поэтому дети мочатся в постель.
Для больных с первичным ночным энурезом характерна никтурия, низкий удельный вес мочи в ночных порциях при проведении пробы по Зим-ницкому. Осмолярность мочи в ночных порциях ниже, чем в дневных. Концентрация АДГ в плазме крови, при исследовании в дневные часы, довольно часто находится в пределах нормы, а если и выявляется её снижение, то оно незначительно. Сниженную концентрацию АДГ в плазме крови чаще выявляют в вечерние и ночные часы. Назначение больным первичным ночным энурезом синтетических аналогов АДГ приводит к излечению у 70-80% пациентов [Темерина Е.А., 1998].
Нефрогенный несахарный диабет (несахарный диабет, не чувствительный к АДГ). В основе заболевания лежит отсутствие чувствительности эпителия почечных канальцев к АДГ. При взаимодействии АДГ с рецепторами почечных канальцев не образуется цАМФ, поэтому не происходит активация протеинкиназы А и внутриклеточный эффект АДГ не реализуется. Болеют преимущественно лица мужского пола. Заболевание наследуется как сцепленный с Х-хромосомой признак. Изменения лабораторных показателей и функциональных тестов аналогичны тем, что выявляют при несахарном
диабете. Для нефрогенного несахарного диабета характерна нормальная или повышенная концентрация АДГ в плазме крови. При проведении теста с вазопрессином отсутствует повышение уровня цАМФ в моче после его введения.
При нефрогенном несахарном диабете применение препаратов АДГ неэффективно. Тиазидные диуретики в сочетании с длительным ограничением поваренной соли в диете могут дать хороший клинический результат. Необходимо проводить коррекцию гипокалиемии и гиперкальциемии под контролем концентрации калия и кальция в сыворотке крови.
Синдром неадекватной секреции вазопорессина (синдром Пархона) — самый частый вариант нарушения секреции АДГ. Характеризуется олигури-ей, (постоянной или периодической), отсутствием жажды, наличием общих отёков, нарастанием массы тела и высокой концентрацией АДГ в плазме крови, неадекватной уровню осмолярности.
Данный синдром может развиться при патологии ЦНС, в частности при менингите, энцефалите, опухолях и абсцессах мозга, субарахноидальных кровоизлияниях, черепно-мозговых травмах, а также может быть обусловлен пневмонией, туберкулёзом, ОПП, психозами, некоторыми ЛС (вин-кристином, карбамазепином и др.). В некоторых случаях неадекватная секреция АДГ возможна при гипотиреозе. Механизм нарушения секреции АДГ обусловлен непосредственным поражением гипоталамуса. Иногда причину неадекватной секреции АДГ установить не удаётся. В плазме крови выявляют снижение концентрации натрия (менее 120 ммоль/л); если она становится ниже 110 ммоль/л, развивается неврологическая симптоматика — ступор, возможны судороги. Осмолярность плазмы низкая (менее 270 мосм/л), возможно развитие гипоосмолярной комы. При исследовании суточной мочи отмечают повышенное выделение натрия из организма. Обнаруживают повышенное содержание АДГ в плазме крови по отношению к её осмолярности, уменьшенную концентрацию альдостерона, сниженный ответ при проведении теста угнетения секреции АДГ путём водной нагрузки.
Эктопическая секреция АДГ возможна при самых различных опухолях. Наиболее часто эктопическая секреция АДГ сопровождает бронхогенный рак лёгкого, злокачественные опухоли поджелудочной, вилочковой желёз, двенадцатиперстной кишки. Изменение лабораторных показателей аналогично таковым при синдроме неадекватной секреции вазопорессина.
Комплексная оценка результатов лабораторных исследований у больных с различными формами полиурии представлена в табл..
Таблица Оценка лабораторных показателей у больных с полиурией
Таблица Оценка лабораторных показателей у больных с полиурией

Окончание табл.
Тест стимуляции АДГ путём ограничения приёма воды до введения вазопрессина
Окончание табл.